Po przyjęciu doraźnego leku przeciwbólowego pacjenci oczekują szybkiego i skutecznego uśmierzenia bólu. W celu osiągnięcia tego efektu oraz w celu dalszego wspomagania działania leków przeciwbólowych zawierających ibuprofen o udowodnionym działaniu istnieją zasadniczo dwa sposoby: skojarzenie go z innymi substancjami, takimi jak koanalgetyk kofeina, lub opracowanie ibuprofenu do postaci soli lizyny, co ma na celu przyspieszenie jego wchłaniania do krwioobiegu (co prowadzi do szybszego uśmierzenia bólu).
 Polska
PolskaFarmakokinetyka ibuprofenu: porównanie stałego skojarzenia ibuprofenu plus kofeiny z lizynianem ibuprofenu i kwasem ibuprofenowym
Wyniki dwóch badań z zastosowaniem pojedynczej dawki (randomizowanych, prowadzonych w jednym ośrodku, krzyżowych, prowadzonych metodą otwartej próby)
Jednoznacznie ustalono nadrzędną skuteczność ibuprofenu (400 mg) w skojarzeniu z kofeiną (100 mg) w porównaniu z samym ibuprofenem (400 mg) [1]. W dwóch badaniach klinicznych badano również farmakokinetykę ibuprofenu w skojarzeniu oraz farmakokinetykę lizynianiu ibuprofenu, w obydwu przypadkach na czczo (>10 godzin na czczo), jak również po spożyciu standardowego śniadania [2].
Metody
Przeprowadzono dwa badania kliniczne, każde z udziałem 36 uczestników. W pierwszym badaniu (NCT01879371) farmakokinetykę ibuprofenu w preparacie złożonym zawierającym kofeinę porównano z farmakokinetyką ibuprofenu (w postaci kwasu lub lizynianiu) zawartego w dwóch preparatach porównawczych. Preparaty badane przyjmowano po >10 godzinach bycia na czczo, w czasie których dozwolone było tylko picie wody.
W drugim badaniu (NCT02629354) farmakokinetykę ibuprofenu w preparacie złożonym porównywano z farmakokinetyką ibuprofenu (w postaci lizynianu) po spożyciu standardowego śniadania.
Te badania z zastosowaniem pojedynczej dawki były randomizowanymi, prowadzonymi w jednym ośrodku, badaniami krzyżowymi, prowadzonymi metodą otwartej próby. Kluczowymi parametrami, które mierzono, były maksymalne stężenie w osoczu (Cmax), czas do jego osiągnięcia (Tmax) oraz całkowita ekspozycja (AUC0-t). Parametry te mierzono również dla kofeiny. Metody analityczne i statystyczne odpowiadały standardom [2].
Wyniki
Po przyjęciu na czczo uzyskano oczekiwane wyniki: ibuprofen w postaci lizynianu był wchłaniany szybciej niż kwas ibuprofenowy (z preparatu złożonego lub z preparatu zawierającego tylko ibuprofen); mimo podobnej ekspozycji maksymalne stężenie w osoczu było większe (patrz tabela).
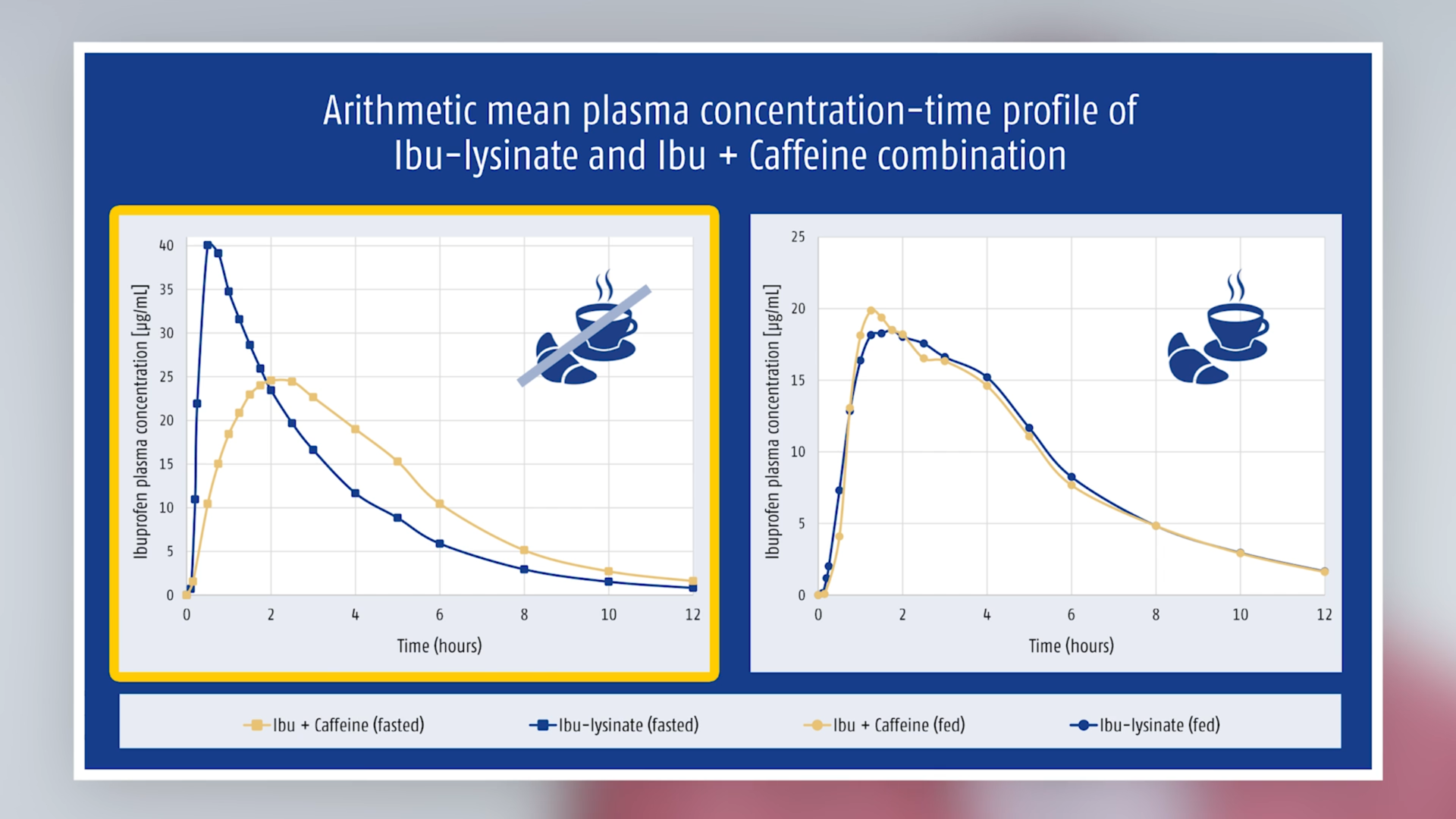
Inny obraz wyłania się w przypadku przyjęcia po standardowym śniadaniu, tzn. w warunkach nie na czczo: w tych warunkach stężenie ibuprofenu w osoczu z preparatu złożonego było większe niż z lizynianu ibuprofenu, a czas do osiągnięcia maksymalnego stężenia w osoczu był krótszy (patrz tabela i rycina 1). Różnica między stanem na czczo/nie na czczo również była znacznie mniejsza niż w przypadku lizynianiu ibuprofenu (rycina 2).
Ryc. 1. Średnia arytmetyczna profili czasu Średniego stężenia w osoczu dla ibuprofenu i kofeiny z preparatu złożonego.
Ryc. 2. Średnia arytmetyczna profili czasu Średniego stężenia w osoczu dla ibuprofenu (w postaci lizynianu).
Omówienie i wyniki
Zgodnie z definicją europejskich organów nadzoru nad lekami termin „na czczo” oznacza, że osoba badana w badaniu nie spożywa żadnych posiłków przez co najmniej 8 godzin przed i 4 godziny po przyjęciu produktu eksperymentalnego, pije jedynie wodę niegazowaną, oraz przez jedną godzinę przed i po przyjęciu nie wolno jej nic pić. Produkty eksperymentalne należy przyjmować, popijając dokładnie 150 ml wody [3]. W tych standaryzowanych warunkach można całkiem dobrze porównać różne badania, aczkolwiek warunki te różnią się bardzo od życia codziennego.
Leków przeciwbólowych nie przyjmuje się zazwyczaj w warunkach, które odpowiadają standardowym wymogom organów nadzorczych dla warunków „na czczo”. W celu osiągnięcia tego stanu dana osoba musiałaby przyjmować lek przeciwbólowy przed śniadaniem (i tylko jeśli nie spożyła wieczornego posiłku zbyt późno!) i musiałaby również rezygnować z samego śniadania. Są to jedyne warunki, kiedy można udowodnić szybsze wchłanianie (i szybsze osiąganie maksymalnego stężenia w osoczu) ibuprofenu w postaci lizynianu w porównaniu z kwasem ibuprofenowym. Starsze dane pokazują, że po standardowym śniadaniu lizynian ibuprofenu i kwas ibuprofenowy mają podobne właściwości farmakokinetyczne, tzn. lizynian ibuprofenu nie wiąże się z żadnymi korzyściami [4]. Najnowsza publikacja wykazuje, że ibuprofen z preparatu złożonego zawierającego kofeinę jest wchłaniany z żołądka w warunkach nie na czczo szybciej i osiąga większe maksymalne stężenie w osoczu niż lizynian ibuprofenu [2].
Piśmiennictwo
- Weiser et al. Efficacy and safety of a fixed-dose combination of ibuprofen and caffeine in the management of moderate to severe dental pain after third molar extraction. Eur J Pain. 2018;22(1):28–38. doi: 10.1002/ejp.1068.
- Weiser et al. Pharmacokinetic Properties of Ibuprofen (IBU) From the Fixed-Dose Combination IBU/Caffeine (400/100 mg; FDC) in Comparison With 400 mg IBU as Acid or Lysinate Under Fasted and Fed Conditions-Data From 2 Single-Center, Single-Dose, Randomized Crossover Studies in Healthy Volunteers. Clin Pharmacol Drug Dev. 2019;8(6):742–753. doi: 10.1002/cpdd.672.
- EMA GUIDELINE ON THE INVESTIGATION OF BIOEQUIVALENCE, 2010 https://www.ema.europa.eu/en/documents/scientific-guideline/guideline-investigation-bioequivalence-rev1_en.pdf (accessed 05.12.2019)
- Klüglich et al. Ibuprofen extrudate, a novel, rapidly dissolving ibuprofen formulation: relative bioavailability compared to ibuprofen lysinate and regular ibuprofen, and food effect on all formulations. J Clin Pharmacol. 2015;45(9):1055–61.
Konflikt interesów: T. Weiser jest pracownikiem firmy Sanofi.
Ujawnienie: Publikacja sfinansowana przez Sanofi Aventis Deutschland GmbH.